败血症中,细胞“隧道”帮心脏细胞传递“能量工厂”
作者: aeks | 发布时间: 2026-03-30 12:02 | 更新时间: 2026-03-30 12:02
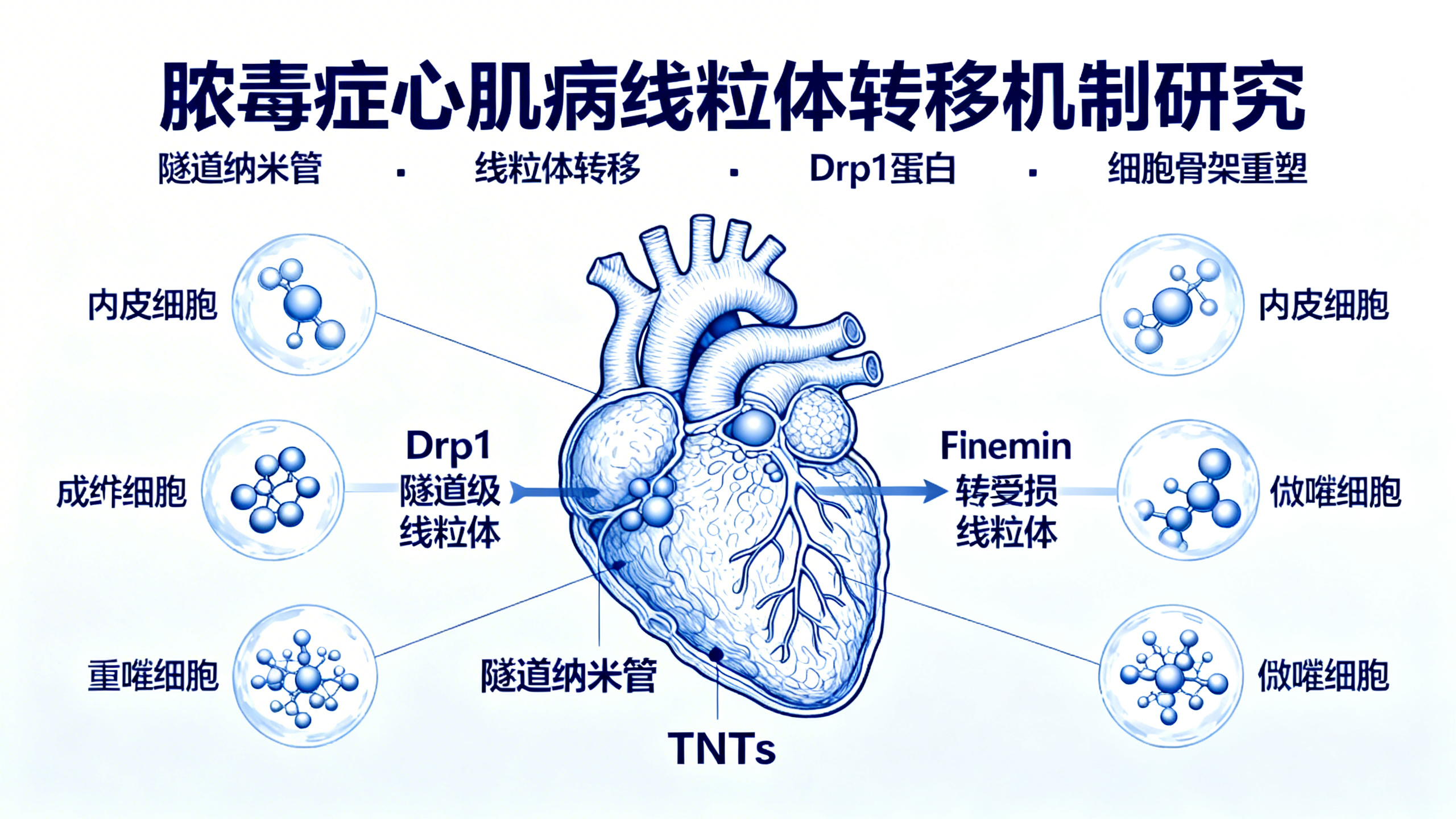
脓毒症是一种危及生命的全身性感染反应,常导致多器官衰竭,其中约40%的患者会出现心脏功能障碍,表现为心肌收缩力下降和射血分数降低,显著增加死亡风险。过去研究多聚焦于心肌细胞自身的损伤,但本文揭示了一个被长期忽视的关键机制:非心肌细胞(如心脏内皮细胞、成纤维细胞和巨噬细胞)在脓毒症中同样发生深刻改变,并积极参与心脏损伤进程。研究团队利用小鼠盲肠结扎穿刺(CLP)模型模拟严重脓毒症,并结合单细胞RNA测序(scRNA-seq)技术,在单细胞精度上全面绘制了心脏各类细胞在疾病不同阶段的基因表达图谱。结果发现,脓毒症促使心脏内皮细胞、成纤维细胞和巨噬细胞均出现功能性亚群转换——原本代谢活跃、线粒体功能健全的细胞亚群(如Aqp7+内皮细胞、Fmo2+成纤维细胞、Hpgd+巨噬细胞)逐渐消失,取而代之的是大量线粒体功能受损、氧化应激升高、炎症加剧的新型亚群(如Cxcl2+/Metal+内皮细胞、Lcn2+成纤维细胞、Metal+/Ccr2+巨噬细胞)。这些异常亚群在线粒体呼吸能力、脂肪酸代谢及抗氧化能力等方面均显著下降,且电镜观察证实其内部堆积着大量结构破损的线粒体。进一步研究发现,这些受损线粒体并非原位产生,而是从邻近的心肌细胞“转移”而来。研究人员通过超高分辨率显微成像(包括3D结构光照明显微镜、扫描电镜等)直接观察到:脓毒症中心肌细胞会伸出大量‘隧道纳米管’(TNTs),这些纳米级管道可跨越较长距离,将受损线粒体主动转运至周围各类驻留细胞。而驱动这一过程的核心分子是Drp1蛋白——它不仅调控线粒体分裂,更在脓毒症压力下发生构象改变,直接与细胞骨架蛋白Filamin(调控肌动蛋白网络)和Kinesin(驱动微管运输)结合,从而重塑细胞骨架,促进TNT的形成与延伸。为验证其因果关系,研究者构建了心肌细胞特异性Drp1基因敲除小鼠。结果显示:敲除Drp1后,TNT数量大幅减少,心肌细胞向周围细胞的线粒体转移被有效阻断;相应地,内皮细胞、成纤维细胞和巨噬细胞不再出现代谢紊乱和炎症激活,其线粒体呼吸功能得以维持,最终心脏整体收缩功能也得到显著改善。这表明,Drp1介导的TNT通路并非简单的‘废物转运’,而是一个具有病理放大效应的关键环节:心肌细胞本意是通过排出受损线粒体进行自我保护,但这一行为却意外地将损伤‘传染’给了邻居细胞,形成恶性循环。因此,靶向干预Drp1-TNT轴,有望成为治疗脓毒症心肌损伤的新策略。