疟原虫如何“搭建骨架”并分裂出新细胞
作者: aeks | 发布时间: 2026-03-18 18:03 | 更新时间: 2026-03-18 18:03
学科分类: 基础医学
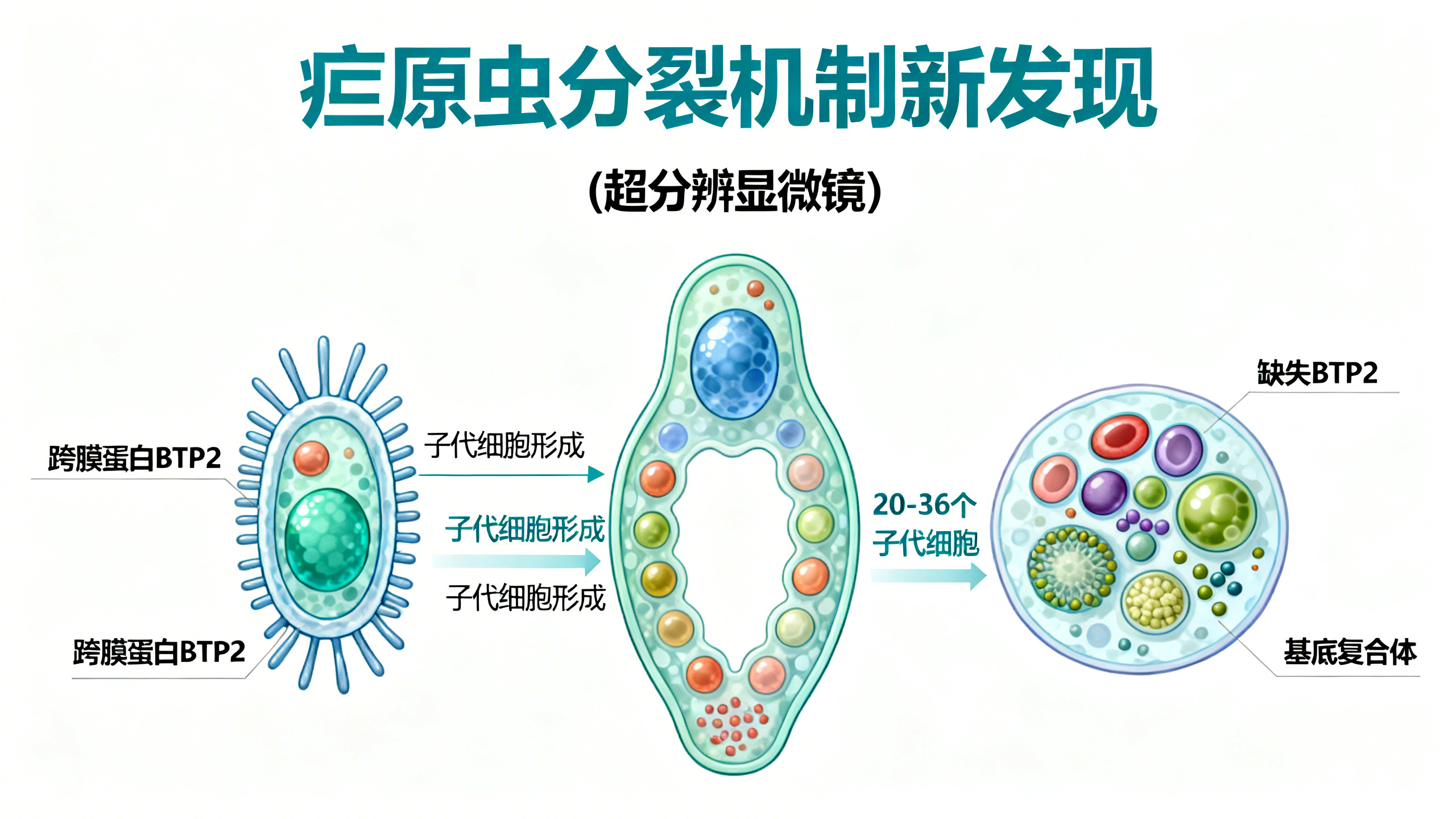
本文研究了疟原虫(恶性疟原虫)无性繁殖过程中基底复合体的组装机制。基底复合体是疟原虫分裂时形成多个子代细胞所必需的核心结构,其功能类似于高等生物细胞分裂中的收缩环。过去对其如何组装知之甚少。研究团队利用超分辨显微技术(DNA-PAINT和超分辨膨胀显微镜U-ExM),系统追踪了三种跨膜蛋白——BTP1、BTP2和BLEB——在基底复合体发育全过程中的精确定位与动态变化。结果发现:BTP2并非如原先设想的那样起‘桥梁’作用(连接基底复合体与细胞膜),而是在基底复合体组装后期专门调控成对结构的分离;若缺失BTP2,基底复合体虽仍能收缩,却无法完成个体化分离,导致多个子代细胞被包裹在同一层细胞膜内,形成含2个或3个细胞核及相应细胞器的‘多核子代细胞’,甚至出现子代细胞在基底部相互粘连的现象。相比之下,BTP1虽也影响子代细胞形成,但其功能部分依赖于BTP2——BTP2缺失后,BTP1无法正确定位于基底复合体,说明BTP2在组装中起主导和上游作用。此外,研究重新定义了BLEB蛋白的功能:它并不属于基底复合体本身,而是标记了一类特殊的质膜区域——该区域紧邻基底复合体,但会被主动排除在新生子代细胞的细胞膜之外,最终归入残余体(母细胞残留物)。这提示基底复合体不仅驱动膜包裹,还像‘筛子’一样精准区分新旧质膜成分。综合所有发现,作者提出了一个三步模型:基底复合体首先呈C形启动,继而扩大并闭合为环状,最后在BTP2介导下完成成对结构的分离;只有完成最后一步,才能确保每个子代细胞独立成形。该研究首次揭示了跨膜蛋白在同步产生数十个子代细胞这一独特分裂模式中的核心调控作用,为理解疟原虫致病机制和开发新型抗疟药物提供了新靶点。