结核分枝杆菌中一种“外膜间隙蛋白组合”如何帮助细菌抵抗药物
作者: aeks | 发布时间: 2026-05-02 21:01 | 更新时间: 2026-05-02 21:01
学科分类: 基础医学 微生物学 生物化学与分子生物学 药学
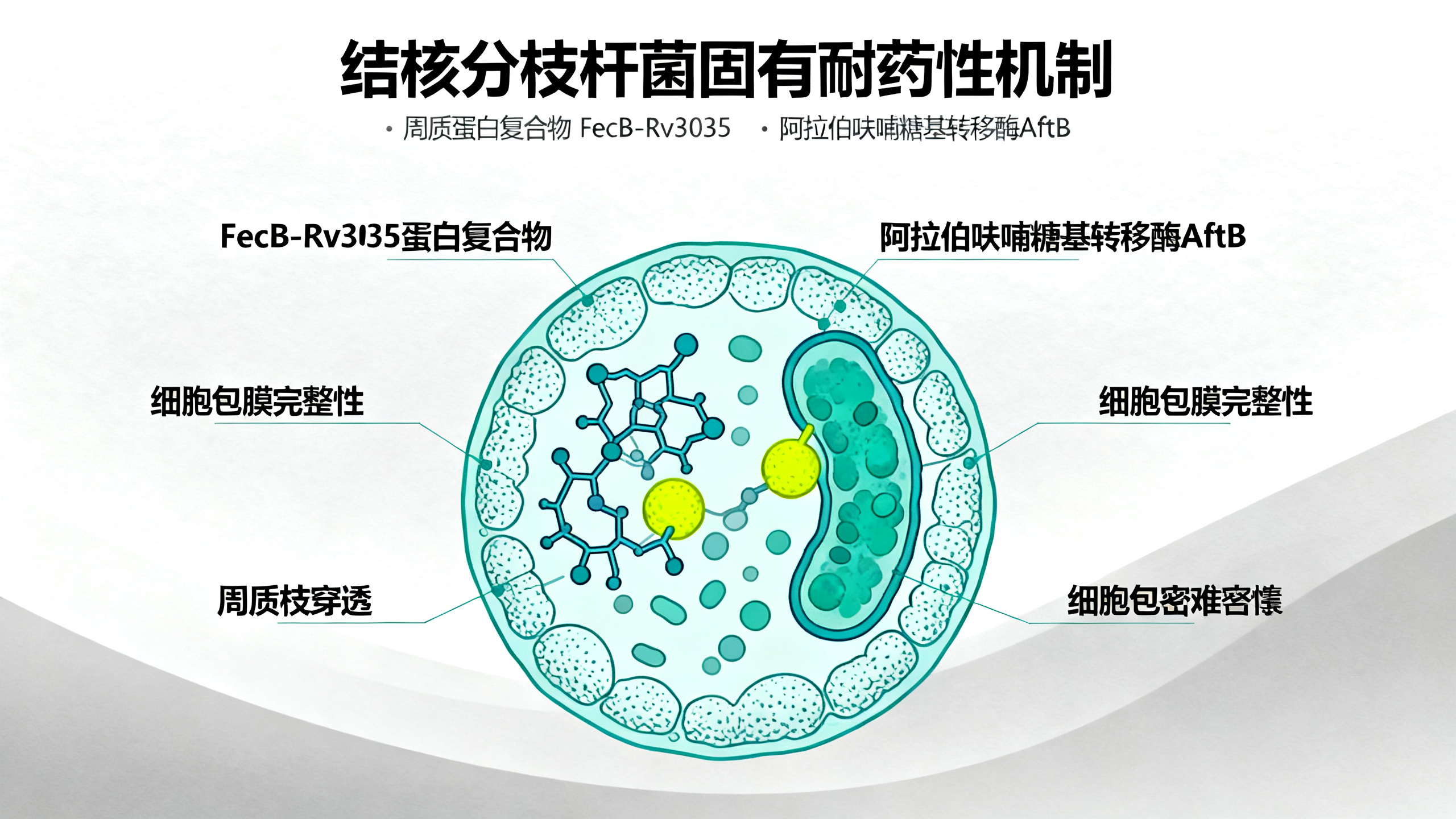
结核分枝杆菌中一种“外膜间隙蛋白组合”如何帮助细菌抵抗药物
结核病仍是全球致死率最高的传染病之一,其难治性主要源于结核分枝杆菌(Mtb)固有的多重耐药性,而这种耐药性很大程度上由其异常致密、难以穿透的多层细胞包膜所决定。本文通过系统研究,首次揭示了一个由周质蛋白FecB和Rv3035组成的新型蛋白复合物,该复合物并非直接参与铁摄取(此前对其功能的主流猜测),而是通过与关键阿拉伯呋喃糖基转移酶AftB相互作用,共同调控细胞包膜核心组分——阿拉伯半乳聚糖(AG)和脂阿拉伯甘露聚糖(LAM)的生物合成。研究团队利用蛋白质互作分析、基因敲除、结构生物学(解析了Rv3035单体及FecB-Rv3035复合物的高分辨率晶体结构)、脂质组学和糖链分析等多种技术证实:缺失FecB或Rv3035会导致AftB酶活性下降,使AG/LAM分子末端阿拉伯糖连接减少;同时造成包膜前体物质(如TMM、TDM和游离分枝菌酸)异常堆积,包膜通透性显著增加,从而使细菌对万古霉素、利福平等多种抗生素变得异常敏感。更重要的是,FecB-Rv3035-AftB三者在遗传上“共必需”,且其物理互作形成了一个功能性的分子桥梁,其中Rv3035如同“支架”,将FecB与AftB精准对接,可能帮助AftB更有效地识别底物或调节其催化活性。动物实验证明,FecB对Mtb在小鼠体内的致病力至关重要。综上,该研究阐明了一种全新的、不依赖于传统靶点的内在耐药机制,将FecB、Rv3035和AftB共同确立为极具潜力的抗结核联合治疗新靶标。