肺癌早期,肺部细胞“变形”能力如何影响肿瘤内部的多样性
作者: aeks | 发布时间: 2026-03-29 18:04 | 更新时间: 2026-03-29 18:04
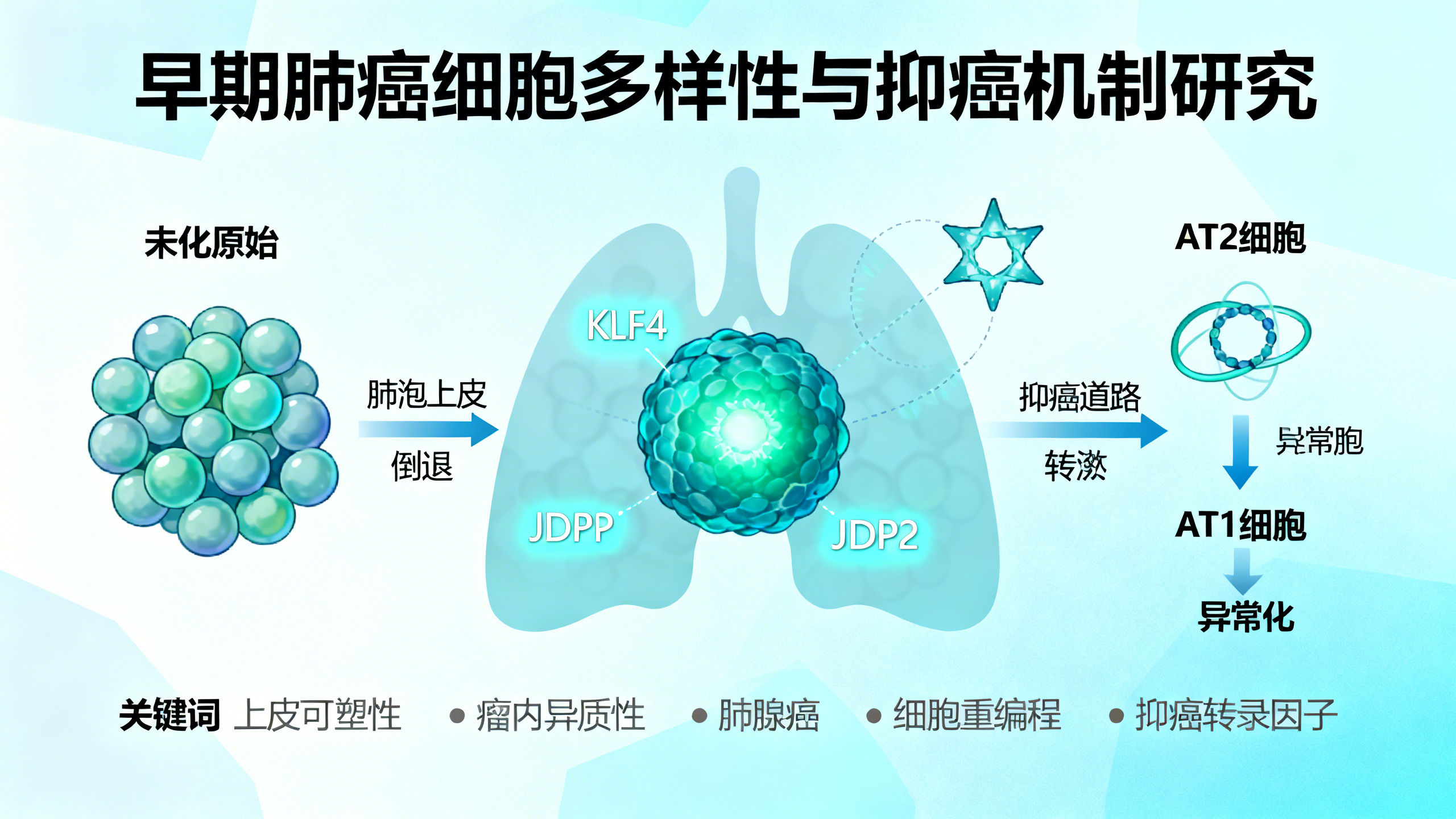
肺癌早期,肺部细胞“变形”能力如何影响肿瘤内部的多样性
本研究利用单细胞测序和空间转录组技术,系统分析了14例早期肺腺癌(包括微浸润性腺癌MIA和Ⅰ期浸润性腺癌IA)患者肿瘤组织(共103,375个细胞),首次揭示:早期肺癌并非均质,而是在肿瘤体积尚小于3厘米时就已形成显著的瘤内转录异质性(ITH)。这种异质性并非主要来自基因突变,而是源于肿瘤细胞自身的‘上皮可塑性’——即细胞主动降低分化程度(去分化),并发生跨谱系转化(如AT2细胞向AT1细胞转化)。研究发现,随着病情从MIA进展到IA,肿瘤细胞逐渐丧失正常肺泡上皮标志物(如AT2/AT1特征基因),这种‘分化程度下降’不仅是疾病进展的关键生物学标志,还能有效预测患者预后:分化程度越低,生存率越差。尤为关键的是,研究识别出一类独特的‘AT2向AT1转化过渡态’细胞(C2簇),这类细胞虽处于转化过程中,却异常激活了p53等抑癌通路,并高表达多种经典抑癌基因,表现出天然的肿瘤抑制潜力。进一步机制挖掘发现,转录因子KLF4和JDP2是驱动这一过渡态形成的核心开关:它们共同调控相关基因,将恶性细胞重编程为这种相对温和、具备抑癌功能的状态。在体外和动物实验中,人为提高KLF4或JDP2的表达,能显著抑制肺癌细胞增殖、迁移和成瘤能力。因此,该研究不仅阐明了早期肺癌异质性的新起源——非遗传性的、由上皮可塑性驱动的细胞状态多样性,更提出了极具前景的治疗新策略:不直接杀死癌细胞,而是通过靶向KLF4/JDP2通路,将恶性细胞‘教育’或‘重编程’为功能受限、生长缓慢甚至具备抑癌活性的过渡态细胞,从而实现对早期肺癌的精准干预。