成年斑马鱼脊髓再生过程中,受损神经元及其周围环境的动态变化
作者: aeks | 发布时间: 2026-03-29 15:01 | 更新时间: 2026-03-29 15:01
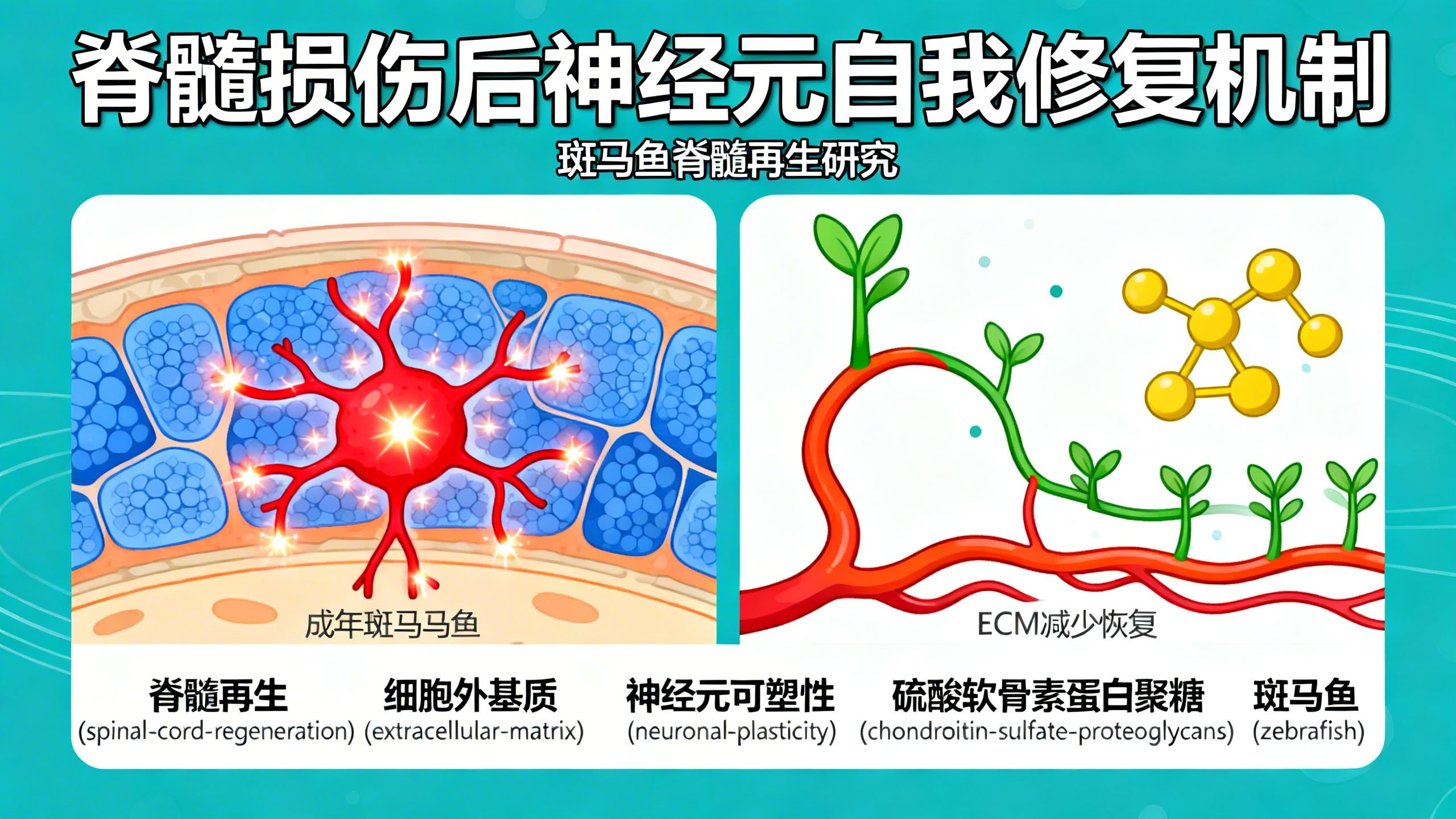
成年斑马鱼脊髓再生过程中,受损神经元及其周围环境的动态变化
本文以具有天然脊髓再生能力的成年斑马鱼为模型,系统揭示了损伤后神经元及其微环境如何通过精密的时间协作实现功能修复。研究聚焦两类关键脊髓神经元(初级运动神经元pMNs和背侧V2a中间神经元dV2a-INs),发现:损伤后3–7天,这些神经元虽结构受损(如树突丢失约50%、轴突断裂),但胞体完好、无细胞死亡;其电活动显著增强——静息膜电位去极化、放电频率升高、适应性降低,且这种变化在14天内完全可逆。进一步证实,这种兴奋性提升主要源于谷氨酸能突触输入增强(包括突触内和突触外持续性谷氨酸释放),而非新突触形成;相反,突触前标志物SV2阳性小点数量反而减少,说明增强的信号来自既有突触的“超常释放”。与此同时,包裹神经元的细胞外基质(ECM)也发生动态重塑:损伤后3–7天,抑制性成分硫酸软骨素蛋白聚糖(CSPGs)大量沉积,形成类似“神经元保护网”的结构;至14天基本恢复常态。尤为关键的是,人为用酶(ChABC)提前降解CSPGs虽能加速早期桥接和轴突生长,却导致后期再生停滞、运动功能恢复变差。这表明CSPG富集的ECM具有双重作用:急性期起“刹车+护盾”作用(限制过度兴奋、防止兴奋毒性),恢复期则转为“支架+引导”作用(稳定结构、支持突触重塑与轴突再生)。综上,脊髓修复并非单一环节发力,而是神经元兴奋性调控、突触可塑性与ECM时序性重构三者紧密耦合的结果。该发现提示:未来针对脊髓损伤的治疗,不能简单清除“抑制性”ECM,而需像调节音量一样,在正确时间、对特定区域进行精准干预。