黏膜黑色素瘤中,特定组织发炎如何让癌细胞“上瘾”
作者: aeks | 发布时间: 2026-04-27 12:02 | 更新时间: 2026-04-27 12:02
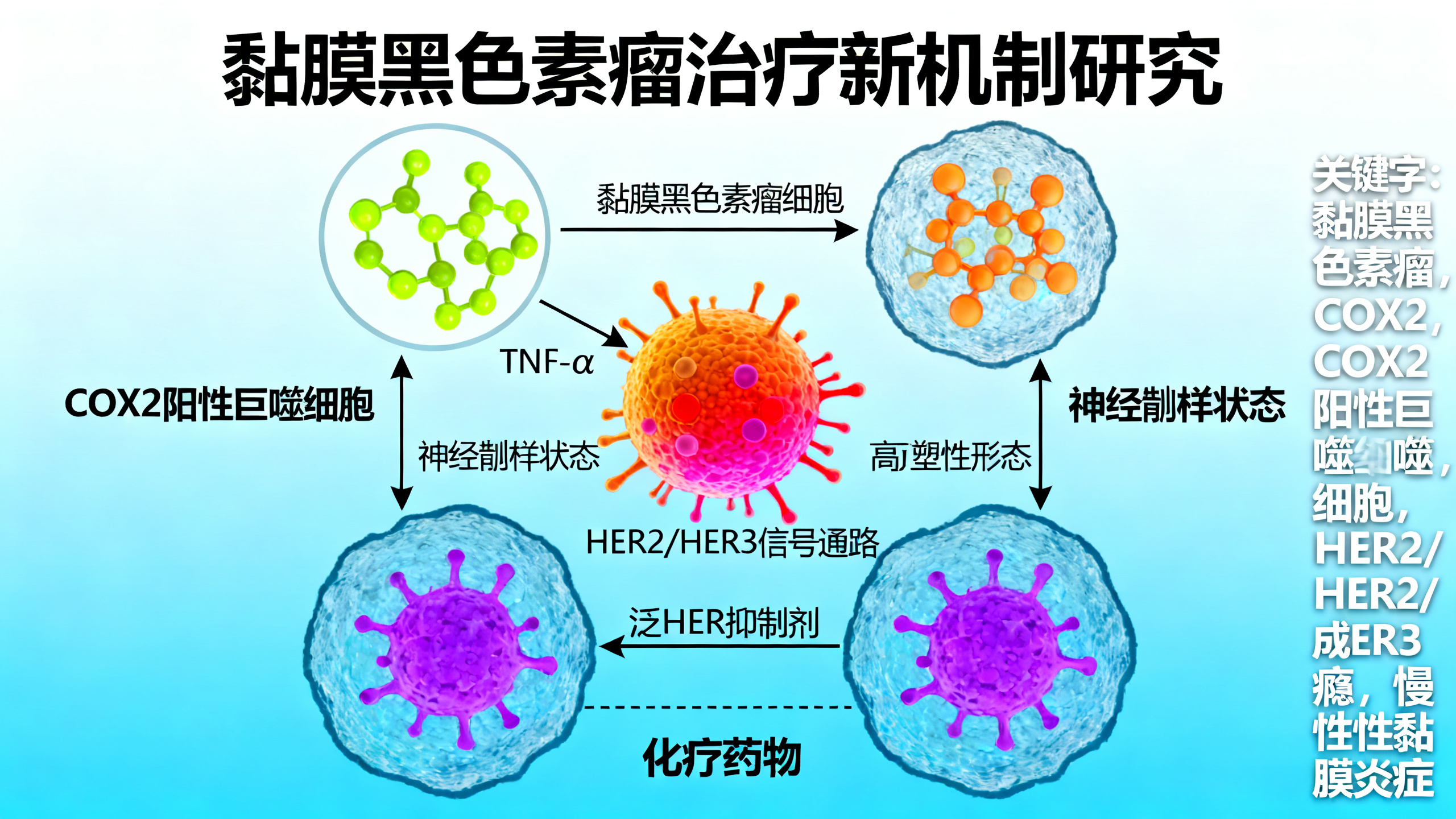
黏膜黑色素瘤(MM)是一种罕见但极具侵袭性的皮肤外黑色素瘤,多发于口腔、鼻腔等黏膜部位。与常见的皮肤黑色素瘤不同,MM对现有靶向治疗和免疫治疗反应极差,5年生存率仅约14%,远低于皮肤型的90%以上。本研究通过整合分析9例患者的单细胞测序和45例患者的 bulk RNA测序数据,并结合大量实验验证,系统揭示了MM恶性进展的关键机制:首先,临床观察发现超过60%的MM肿瘤呈低色素或无色素状态(而皮肤黑色素瘤中该比例不足2%),且色素越少,患者预后越差;进一步分析表明,这种色素丢失并非随机现象,而是癌细胞主动转变为一种类似胚胎期神经嵴干细胞(NCSC)的“去分化”状态,该状态具有高度可塑性、强耐药性和强转移潜能。其次,机制上,黏膜组织本身易发生慢性炎症(如牙周炎),炎症会诱导产生一类特殊的COX2阳性巨噬细胞——它们不同于正常组织中起修复作用的C1Q+巨噬细胞,而是持续分泌促炎因子TNF-α;TNF-α作用于癌细胞后,不仅直接驱动其进入神经嵴样状态,还同步上调癌细胞表面的HER2和HER3受体;更关键的是,这些COX2+巨噬细胞自身还分泌多种HER家族配体(如NRG1),从而形成“双向激活环”,使癌细胞对HER2/HER3信号产生强烈依赖(即“致癌成瘾”)。最后,针对这一弱点,研究人员使用泛HER抑制剂(如阿法替尼)联合传统化疗药(如多柔比星),在细胞实验、类器官模型及患者来源的异种移植(PDX)小鼠模型中均证实:该组合能特异性清除神经嵴样癌细胞,逆转耐药,显著抑制肿瘤生长,且安全性良好。该研究首次阐明了黏膜特异性炎症如何通过微环境—癌细胞互作塑造MM的独特恶性表型,并为这一目前尚无标准有效治疗方案的致命疾病,提供了精准、可转化的新治疗策略。