用“冷等离子体”技术打造的纳米疫苗,实现精准时空免疫,激活抗癌能力
作者: aeks | 发布时间: 2026-04-18 18:02 | 更新时间: 2026-04-18 18:02
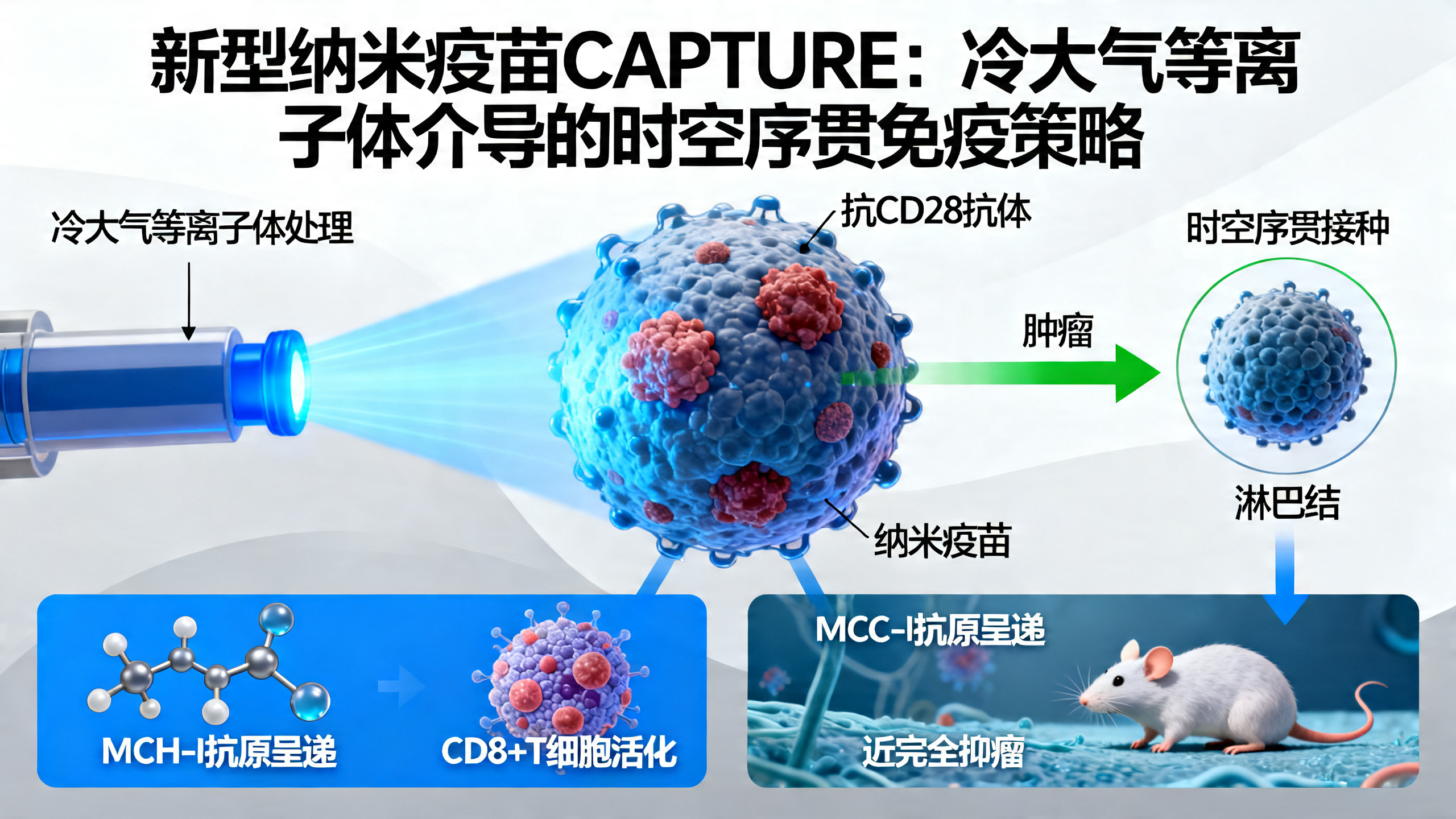
用“冷等离子体”技术打造的纳米疫苗,实现精准时空免疫,激活抗癌能力
癌症免疫治疗常受限于肿瘤抗原呈递不足和免疫抑制微环境。本研究开发了一种名为CAPTURE的仿生纳米疫苗:先用冷大气等离子体(CAP)处理肿瘤细胞,再将其制成纳米囊泡,并在其表面装载抗CD28抗体(αCD28)。CAP处理通过p62介导的自噬通路显著提升肿瘤细胞MHC-I分子表达,从而更全面地呈现多种肿瘤内部抗原(而不仅是膜蛋白抗原);同时,表面αCD28可绕过传统抗原提呈细胞(APC),直接向初始CD8+ T细胞提供共刺激信号,避免被CTLA-4通路抑制。研究进一步设计了“时空序贯免疫”(SSI)策略:先皮下注射启动免疫(靶向淋巴结),再静脉注射加强(靶向肿瘤),实现全身免疫激活与肿瘤微环境重塑。在多种小鼠肿瘤模型中,CAPTURE显著抑制肿瘤生长,机制包括:扩大杀伤性T细胞克隆多样性、增强CXCR3受体表达以促进T细胞向肿瘤浸润、提高干扰素γ(IFN-γ)分泌、诱导肿瘤相关巨噬细胞向抗肿瘤M1型转化,并减少免疫抑制性调节性T细胞(Tregs)。安全性评估显示其无明显急性炎症毒性。该疫苗不依赖个体化新抗原筛选,是一种普适性强、兼具广谱免疫激活与精准靶向能力的新型癌症免疫治疗技术。