血小板导致心梗时血管细胞能量工厂受损
作者: aeks | 发布时间: 2025-12-06 15:01 | 更新时间: 2025-12-06 15:01
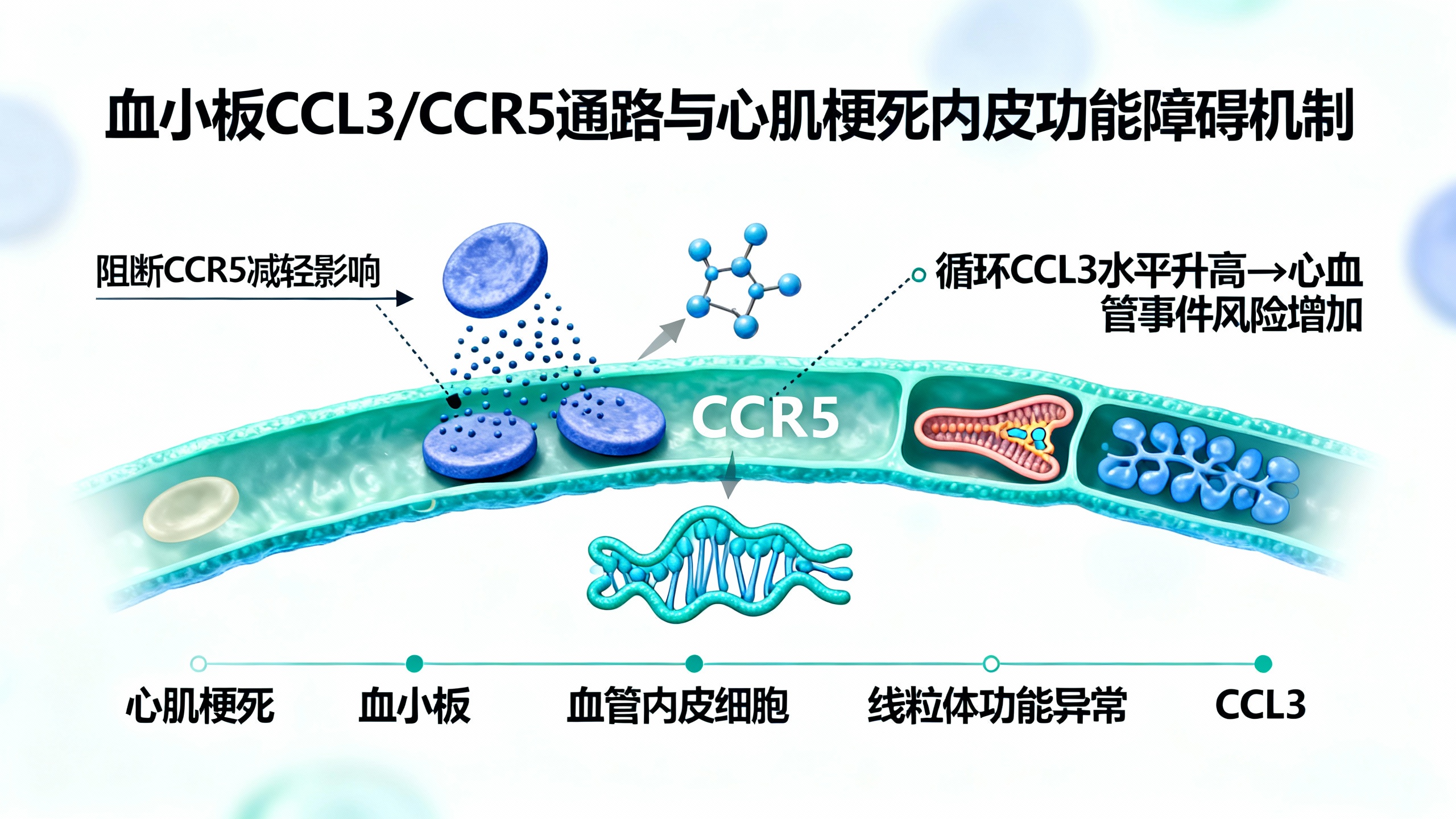
血小板导致心梗时血管细胞能量工厂受损
心肌梗死(MI)是全球心血管疾病死亡的主要原因,因冠状动脉血流中断致心肌不可逆坏死。血管内皮维持抗血栓和抗炎稳态,其功能障碍促进动脉粥样硬化血栓形成。血小板在MI的动脉粥样硬化血栓与炎症中起核心作用,但其引发冠状动脉内皮功能障碍的机制不明。
研究将人冠状动脉内皮细胞与MI患者及对照者的血小板释放物共培养并测序,发现MI血小板释放物致内皮细胞线粒体功能异常:膜电位降低、网络碎裂,氧化磷酸化通路下调。整合血小板转录组数据,鉴定出C-C趋化因子配体3(CCL3)在MI血小板中显著上调,是内皮线粒体功能异常的关键介质。
进一步研究显示,CCL3通过受体CCR5发挥作用。阻断CCR5可减轻线粒体膜电位降低和网络紊乱,阻断CCR1效果不明显,双重阻断无额外益处。机制上,CCL3-CCR5轴通过上调线粒体分裂介质(如DRP1、FIS1)和激活NOX4依赖的活性氧,破坏内皮线粒体完整性。
对261名心血管疾病患者的独立队列研究发现,循环中CCL3水平升高与主要不良心血管事件(MACE,含死亡、MI、中风)风险增加相关。调整风险因素后,高CCL3水平患者MACE风险是低水平者的2.4倍。
综上,血小板来源的CCL3通过CCR5诱导内皮细胞线粒体功能异常,揭示了MI中血小板活化与内皮功能障碍的新机制。CCL3或成为预测临床结局的生物标志物和潜在治疗靶点,为改善MI患者长期预后提供新见解。