Cas9基因编辑为何“怕”甲基化?
作者: aeks | 发布时间: 2026-04-16 09:01 | 更新时间: 2026-04-16 09:01
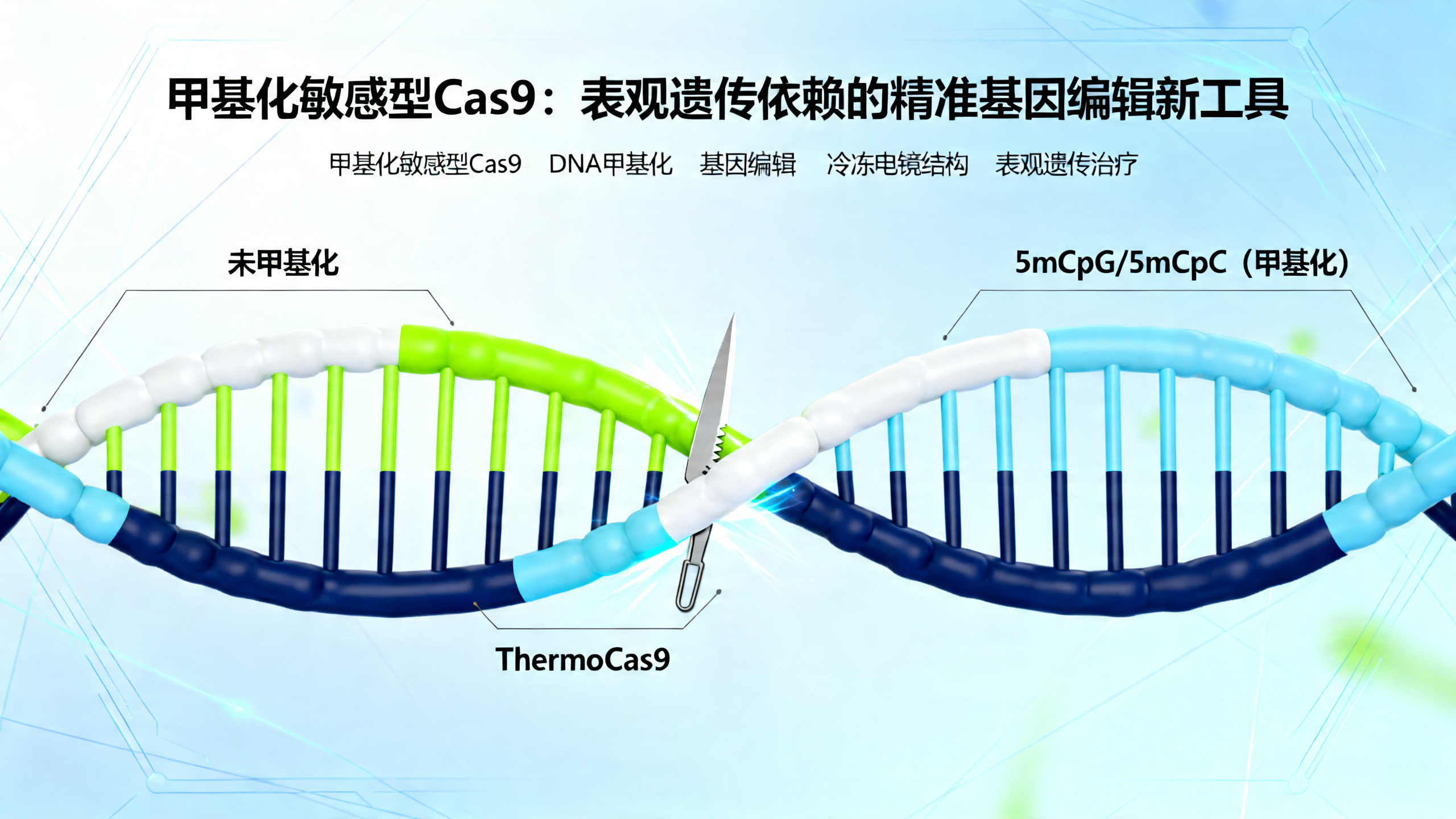
本文介绍了一种名为ThermoCas9的新型细菌CRISPR-Cas9核酸酶,它与传统Cas9不同:它不仅能高效切割DNA,还能“感知”DNA上特定位置的甲基化修饰。具体来说,ThermoCas9识别一种特殊的PAM序列(如5′-NNNNCGA-3′或5′-NNNNCCA-3′),但当该序列中第五位的胞嘧啶(C)被甲基化(形成5mCpG或5mCpC)时,其结合和切割DNA的能力会大幅减弱。研究人员通过冷冻电镜技术,在原子水平上解析了ThermoCas9与DNA结合前(预切割态)和切割后(后切割态)的三维结构(分辨率分别为2.8 Å和2.2 Å),首次揭示了其“拒斥甲基化”的分子机制——甲基基团会直接干扰ThermoCas9蛋白中关键氨基酸(Asp1017和Ser1019)与DNA的紧密接触,导致无法稳定结合。进一步实验表明,这种甲基化敏感性在人类多种细胞系(如HEK293T、HCT116、MCF-7、MCF-10A)中均真实有效:ThermoCas9只对甲基化水平低的DNA位点进行高效编辑,而对高甲基化的位点几乎无作用。研究者还对ThermoCas9进行了蛋白质工程优化,开发出催化活性更强的变体(CE-ThermoCas9),并结合核糖核蛋白(RNP)递送方式,在乳腺癌细胞MCF-7中成功实现了对低甲基化致癌基因GATA3高达78%的靶向编辑。这意味着,未来有望利用ThermoCas9开发出一类全新的“智能”基因编辑疗法——它不仅认准基因序列,更能读懂细胞的表观遗传健康状况,从而只在病变细胞(如因低甲基化而异常激活的癌基因)中启动编辑,极大提升治疗的安全性与精准度。
标签: DNA甲基化 冷冻电镜结构 基因编辑 甲基化敏感型Cas9