马尔堡病毒“钥匙”蛋白及其与人体受体的结合结构
作者: aeks | 发布时间: 2026-03-13 00:02 | 更新时间: 2026-03-13 00:02
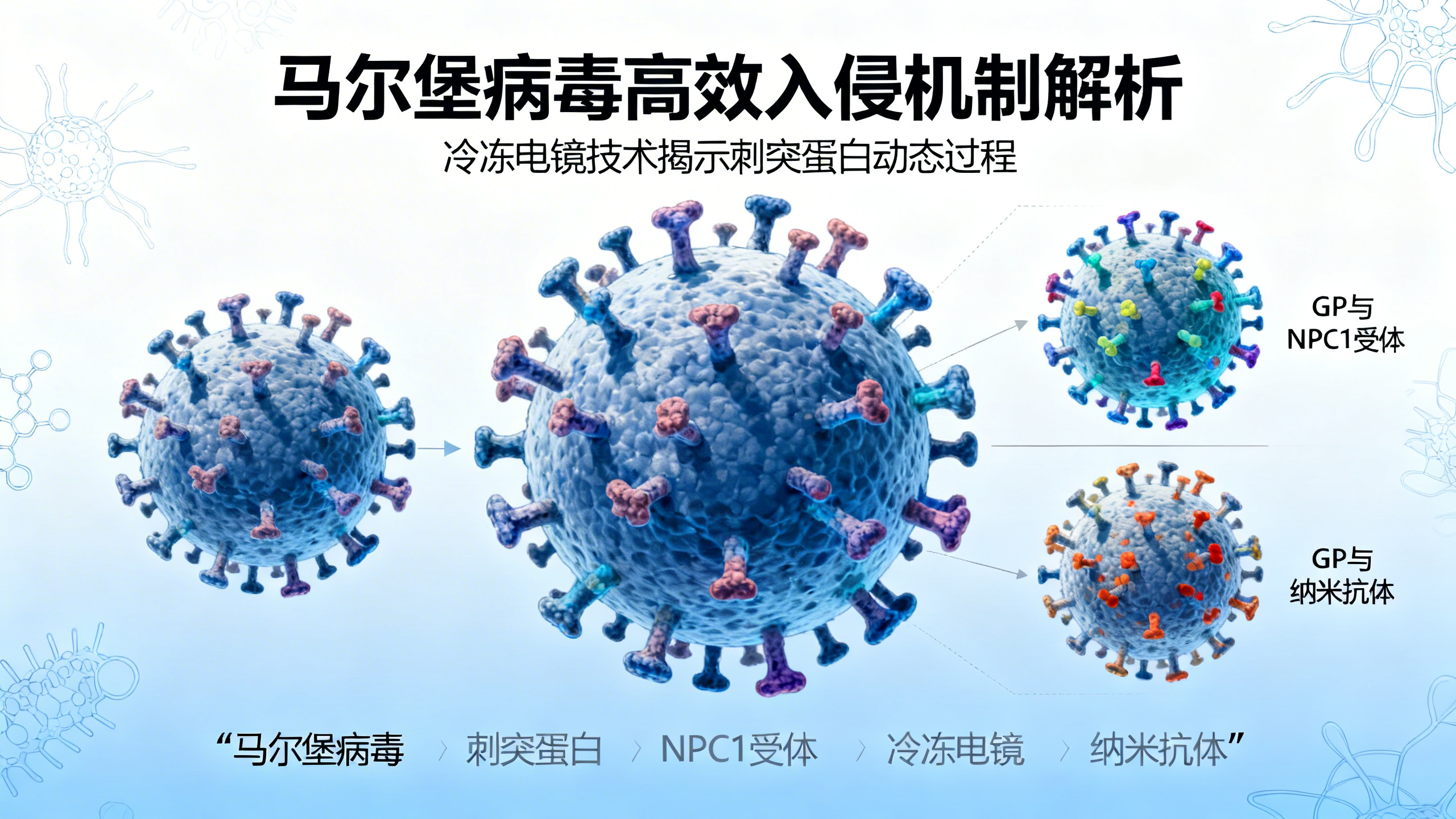
马尔堡病毒(MBV)可引发严重出血热,平均病死率达73%,显著高于埃博拉病毒(EBOV)的44%。目前尚无获批的马尔堡病毒治疗药物或疫苗,防控形势严峻。本研究聚焦于病毒入侵的关键分子——马尔堡病毒糖蛋白(GP),系统比较了其与埃博拉病毒GP在功能与结构上的差异。实验表明,马尔堡病毒GP介导病毒进入人体多种靶细胞(肝癌细胞、血管内皮细胞和巨噬细胞)的效率高达埃博拉病毒GP的12–300倍。为阐明这一高效性背后的机制,研究人员利用冷冻电镜技术,首次成功解析了马尔堡病毒GP的三个关键结构:(1)经蛋白酶剪切后暴露受体结合位点的GPcl(即‘剪切态’);(2)GPcl与人体内体受体NPC1形成的复合物;(3)GP与一种新型中和纳米抗体Nanosota-MB1的复合物。这些结构揭示了三大核心机制:第一,马尔堡病毒GP的‘糖帽’具有部分柔性——它能完全阻挡NPC1受体结合,却仅部分阻碍纳米抗体结合,这种特性可能有助于病毒在免疫逃逸与高效入侵之间取得平衡;第二,NPC1受体以一种全新的角度和方式(多出一个关键结合环)与马尔堡病毒GP结合,亲和力比结合埃博拉病毒GP时高出约11倍;第三,NPC1结合会触发马尔堡病毒GP发生显著构象变化,使蛋白亚基间距增大、相互作用减弱,从而更易启动膜融合过程。此外,研究发现纳米抗体Nanosota-MB1能精准模拟NPC1,插入同一疏水口袋,以超高亲和力阻断病毒与受体结合,且对多种马尔堡病毒毒株均具强效中和能力(IC50约0.5 μg/mL),效力远超已知人源抗体。综上,马尔堡病毒GP凭借其独特的糖帽柔性、更强的受体亲和力及更灵敏的构象响应能力,共同构成了其高效入侵和高致死率的结构基础,也为开发新型抗病毒药物(如基于纳米抗体的疗法)提供了直接依据和重要靶点。