CAR-T细胞治疗难治性重症肌无力:疾病复发的蛋白特征与单细胞基因变化
作者: aeks | 发布时间: 2026-01-20 06:03 | 更新时间: 2026-01-20 06:03
重症肌无力(MG)是一种由B细胞介导的自身免疫性疾病,患者主要表现为骨骼肌波动性无力和疲劳。其发病机制核心是外周耐受机制破坏,导致自身反应性B淋巴细胞成熟为分泌抗体的效应细胞,产生高滴度致病性自身抗体,主要攻击神经肌肉接头处的突触后成分(如乙酰胆碱受体AChR),影响突触传递。B细胞耗竭疗法是MG的重要治疗策略,但现有单克隆抗体(如利妥昔单抗)无法特异性靶向消除产生抗体的浆细胞,且对炎症微环境中的B细胞效果有限,易导致疾病复发,还需频繁输注,增加经济负担和患者依从性挑战。
嵌合抗原受体T细胞(CAR-T细胞)在血液肿瘤治疗中成效显著,正逐步拓展至自身免疫病领域。研究表明,CAR-T细胞可高效清除自身反应性B细胞,重置免疫系统,且安全性良好。既往针对MG的单靶点(BCMA或CD19)CAR-T疗法需重复给药,且未实现完全临床缓解,患者仍依赖免疫抑制剂。鉴于B细胞发育不同阶段表面分子表达变化,单靶点CAR-T难以全面重置B细胞致病功能,因此本研究设计了BCMA/CD19双靶点CAR-T疗法用于难治性MG治疗,并进行了为期1年的综合评估,分析血清蛋白质组学和免疫细胞动态变化,尤其对1例治疗后复发患者的外周血单个核细胞和骨髓样本进行单细胞RNA测序,以阐明潜在复发机制。
研究共纳入6例难治性MG患者(2男4女,年龄32-64岁),均为全身型MG,此前接受多种免疫抑制剂和免疫调节剂治疗但效果不佳。患者基线时QMG评分8-20分,ADL评分6-12分,部分合并胸腺瘤或胸腺增生,部分接受过胸腺切除术。
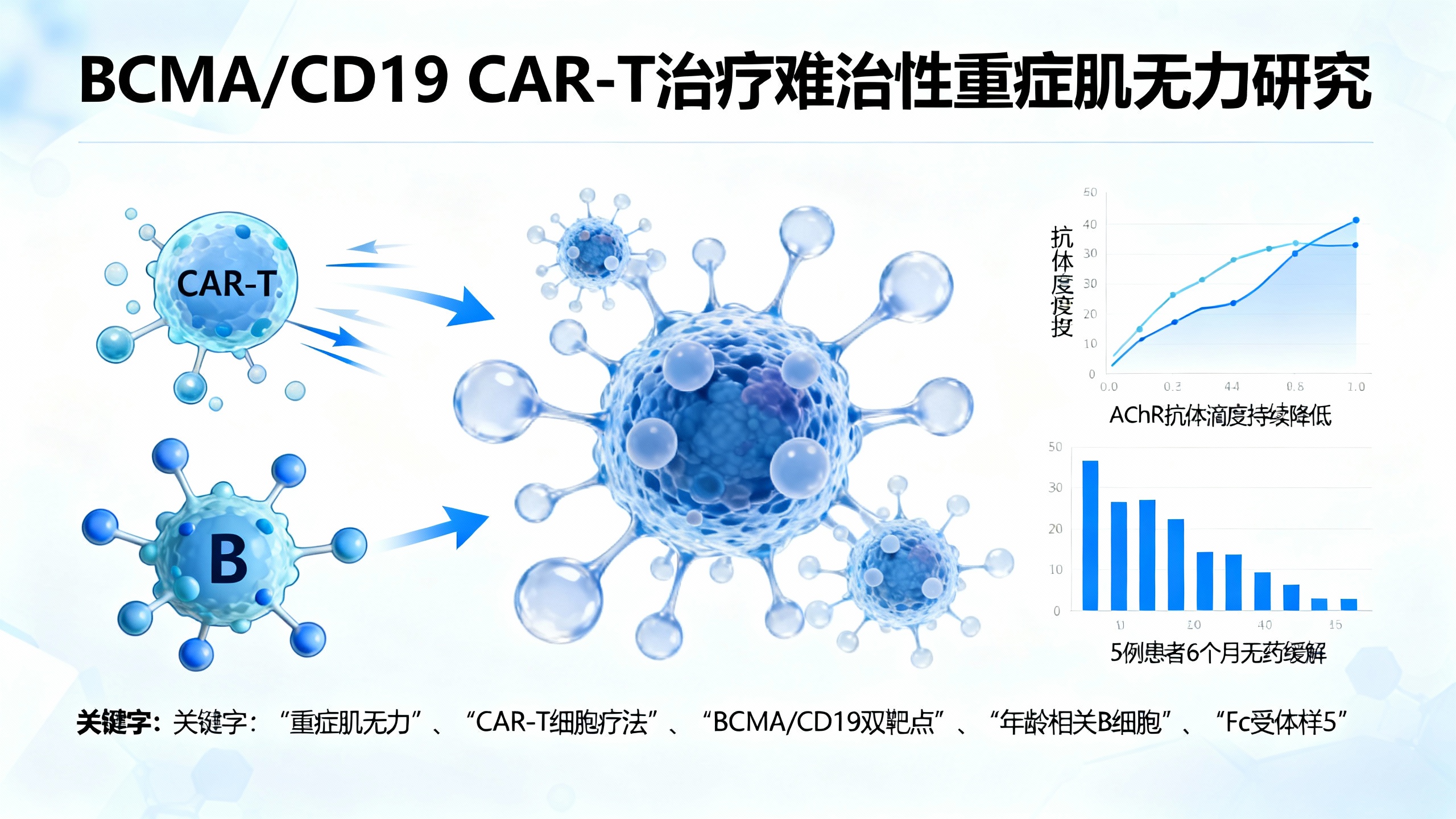
临床疗效方面,CAR-T细胞输注后,5例患者在6个月时达到最小表现状态(MMS)并停用所有药物,ADL评分均为0,部分QMG评分完全正常;12个月随访时,这些患者均维持无药缓解(QMG和ADL评分均为0),部分患者AChR抗体转为阴性或接近阈值。1例患者(P6)在180天内临床改善,但187天出现疾病复发,12个月时ADL评分虽高于180天但仍低于基线。CAR-T细胞输注后14天,所有患者外周B细胞均完全耗竭,部分患者在60-270天出现B细胞重建。
安全性方面,6例患者耐受性良好,未出现CAR-T相关神经毒性综合征(ICANS),2例出现1级细胞因子释放综合征(CRS,表现为轻度发热),经支持治疗缓解;部分患者出现短暂血液学毒性,经对症治疗后迅速改善,未发生严重肝肾等器官功能损害。
蛋白质组学分析显示,CAR-T输注后14天内,促进CAR-T细胞迁移、减少耗竭和增强细胞毒性的细胞因子(如CXCL9、CXCL10、IL-10、IFN-γ)短暂升高,30天开始下降;免疫反应相关抗炎介质、负调控因子和T细胞活化标志物(如LILRB4、LAG3)显著上调,促炎介质TREM1明显下调。
B细胞功能重建方面,重建的B细胞以初始B细胞为主,记忆B细胞和抗体分泌细胞减少,B细胞表面共刺激分子(如OX40L、CD80)表达降低,促炎细胞因子(如IL-6)减少,调节性细胞因子IL-10增加,AChR特异性B细胞显著减少。复发患者(P6)重建后年龄相关B细胞(ABCs)和浆细胞扩增,B细胞活化标志物和促炎细胞因子表达升高。
单细胞测序发现,复发患者外周血ABCs和骨髓浆细胞增加,B细胞差异表达基因富集于B细胞受体信号、活化增殖分化等通路。ABCs在新发MG患者中数量增加且与疾病严重程度正相关,其分化为浆细胞过程中Fc受体样5(FCRL5)表达上调。CAR-T应答患者ABCs中FCRL5表达下调,而利妥昔单抗治疗后复发的MG患者也存在ABCs扩增和FCRL5上调,提示FCRL5可能是复发的新治疗靶点。
综上,本研究首次报道BCMA/CD19双靶点CAR-T疗法在难治性MG中的1年随访数据,5例患者实现无药缓解,安全性良好,为MG治疗提供新策略,同时发现FCRL5有望成为复发患者的潜在靶点。