小细胞肺癌的“亚型特异性”治疗新思路
作者: aeks | 发布时间: 2026-03-31 12:03 | 更新时间: 2026-03-31 12:03
小细胞肺癌(SCLC)约占肺癌病例的15%,虽比例不高,却是致死率最高的癌症之一。它生长迅猛、早期即发生转移、五年生存率极低,且与重度吸烟密切相关。临床上分为局限期(肿瘤局限于一侧胸腔)和广泛期(已扩散至远处),约70%患者确诊时已是广泛期,治疗难度极大。过去认为SCLC起源于肺部神经内分泌(NE)细胞,但新研究发现肺部其他上皮细胞(如基底细胞、簇状细胞)也可能成为起源,说明其起源具有多样性。
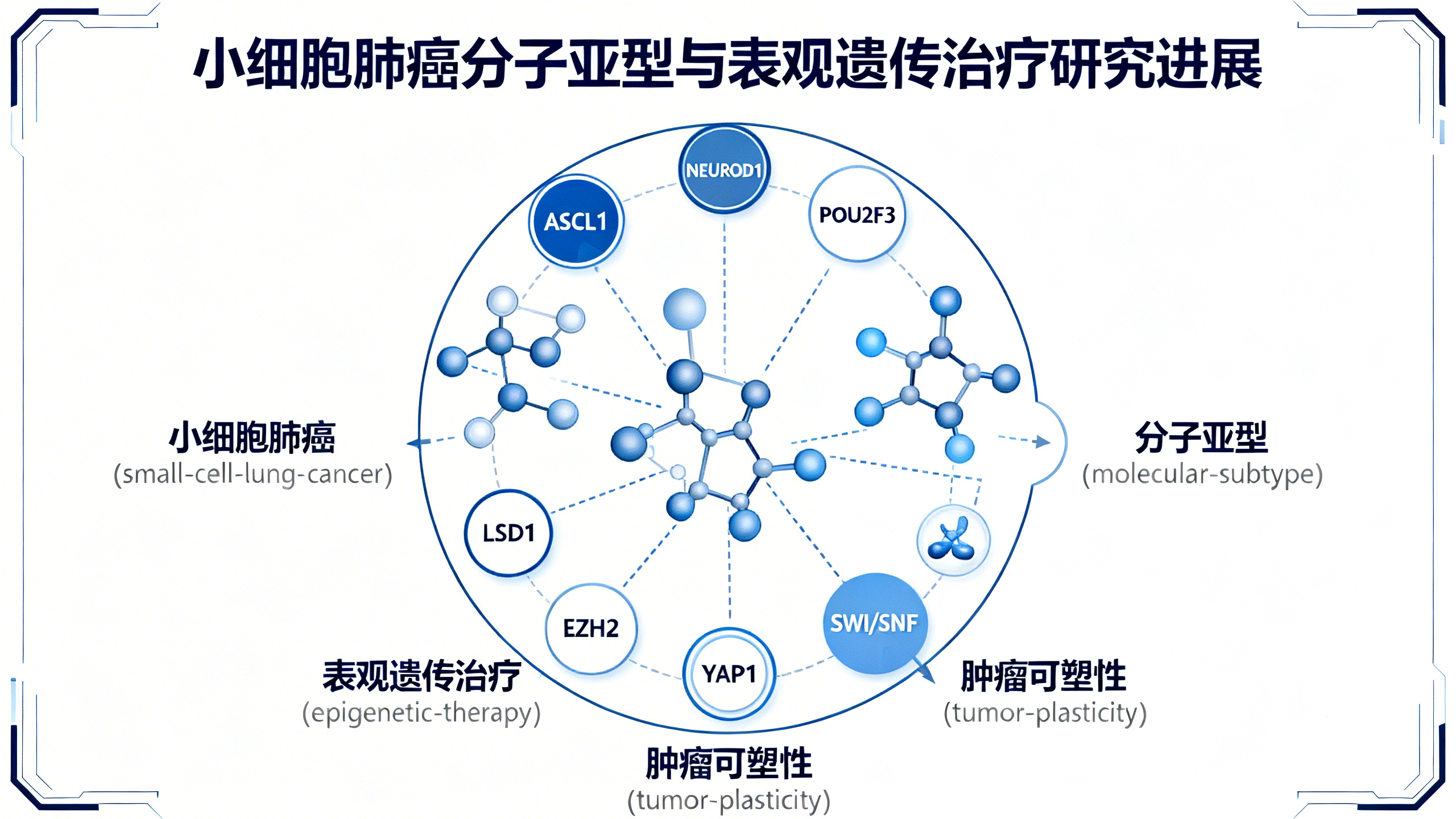
在分子层面,几乎所有SCLC都存在TP53和RB1这两个抑癌基因的失活突变,但很少出现常见的驱动基因激活突变。相反,SCLC高度依赖几个“谱系特异性”转录因子——ASCL1、NEUROD1、POU2F3和YAP1——来维持自身身份和生存。这些因子像“主控开关”,各自调控一套独特的基因表达程序,从而将SCLC划分为四个主要分子亚型:SCLC-A(ASCL1高)、SCLC-N(NEUROD1高)、SCLC-P(POU2F3高)和SCLC-Y(YAP1高)。其中,SCLC-A和SCLC-N属于神经内分泌型(NE-high),而SCLC-P和SCLC-Y则偏向非神经内分泌型(NE-low)。近年还发现了第五种亚型SCLC-I(炎症型),其特点是免疫细胞浸润多、PD-L1表达高,可能更适于免疫治疗;另有研究提出SCLC-AT亚型,由转录因子ATOH1驱动,与肿瘤转移和神经内分泌特征转换相关。
SCLC亚型并非固定不变,而具有高度“可塑性”。例如,在治疗压力下,原本是SCLC-A的肿瘤可能转变为SCLC-N或SCLC-Y,这正是其容易复发和产生耐药的关键原因。MYC基因扩增被证实是推动这种亚型转换的重要驱动力,它通过激活NOTCH信号通路,促使肿瘤从神经内分泌状态转向非神经内分泌状态。此外,SCLC甚至可由非小细胞肺癌(NSCLC)在靶向药治疗后“转化”而来(称为T-SCLC),进一步印证了其强大的适应能力。
正因为各亚型“底子不同”,它们对药物的敏感性也截然不同。例如:SCLC-A亚型高表达抗凋亡蛋白BCL2,因此对BCL2抑制剂(如维奈托克)敏感;SCLC-N亚型常伴MYC扩增,对Aurora激酶抑制剂反应较好;SCLC-P亚型(约占16%)预后较差、化疗效果不佳,但最新研究发现其极度依赖一个此前未被认识的共激活因子POU2AF2(又称OCA-T1),该蛋白与POU2F3形成功能性复合物,共同调控大量下游基因;同时,SCLC-P还高度依赖IGF1R受体和SWI/SNF染色质重塑复合物,抑制这些靶点可有效杀死该亚型肿瘤细胞。而SCLC-I亚型因PD-L1高表达,理论上更适合免疫检查点抑制剂,但实际疗效仍需更多验证。
目前SCLC标准治疗仍是铂类化疗联合依托泊苷,广泛期患者还可加用PD-L1抑制剂(如阿替利珠单抗、度伐利尤单抗)。然而,这些治疗往往仅带来短暂缓解,很快就会复发并耐药。根本原因在于现有疗法未针对SCLC内在的分子异质性和可塑性。因此,未来方向是发展“分型施治”策略:基于患者肿瘤的具体亚型,选择最匹配的靶向药或表观遗传药物。文中特别强调,表观遗传调控(如组蛋白修饰、染色质结构改变)是连接基因型与表型的关键桥梁。已有证据表明,抑制LSD1或EZH2不仅能恢复肿瘤细胞MHC-I抗原呈递能力、增强免疫识别,还能削弱神经内分泌特征;而靶向POU2AF2-SWI/SNF轴则为SCLC-P亚型提供了全新突破口。总之,深入理解SCLC各亚型的“生存依赖”和背后的表观遗传机制,是开发持久有效疗法的核心路径。