阻断DJ-1蛋白,让肿瘤“变友好”,增强免疫治疗效果
作者: aeks | 发布时间: 2026-04-25 15:01 | 更新时间: 2026-04-25 15:01
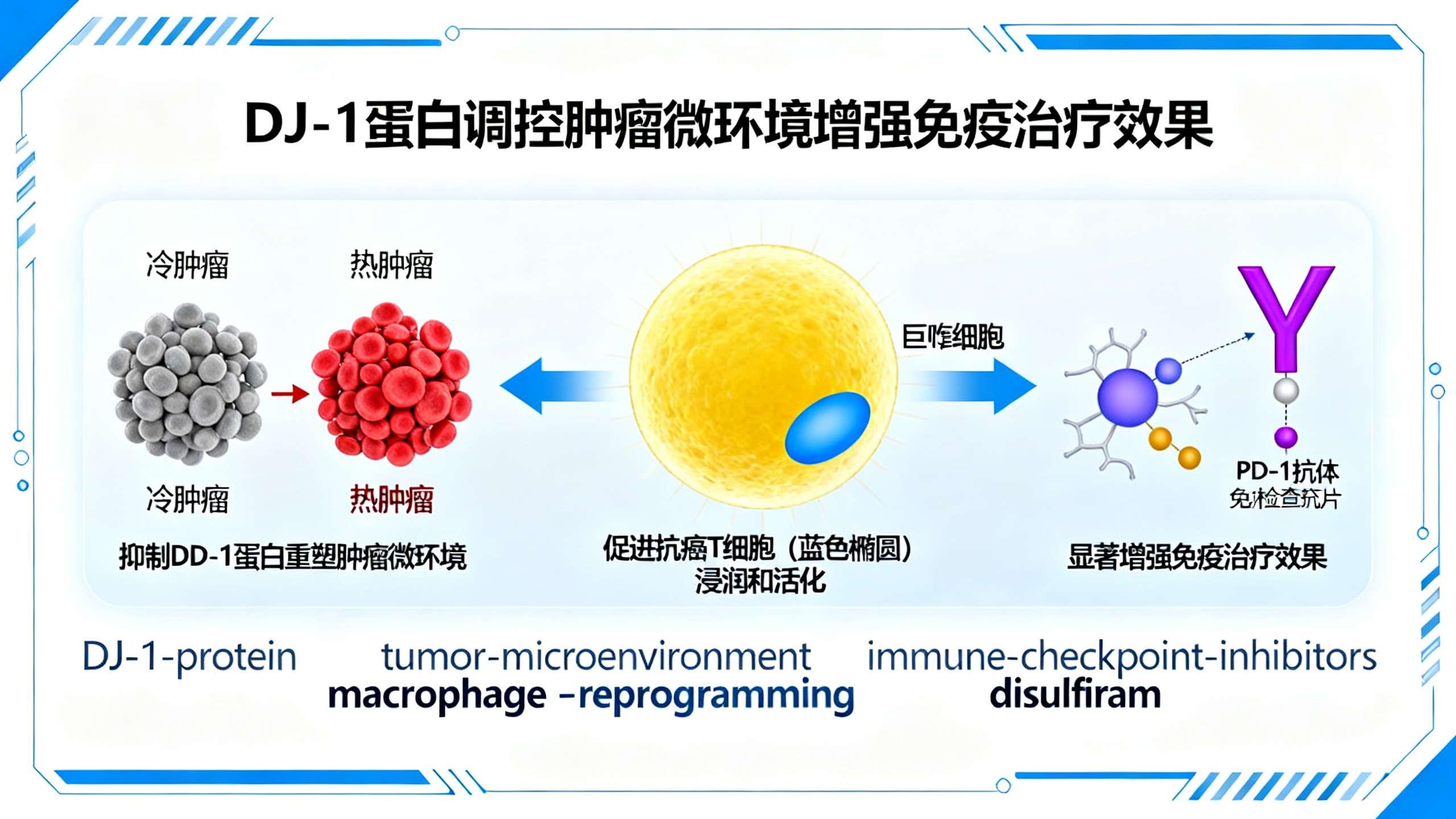
阻断DJ-1蛋白,让肿瘤“变友好”,增强免疫治疗效果
本文报道了一项重要发现:靶向抑制DJ-1蛋白可大幅提升癌症免疫治疗的疗效。目前,以PD-1、TIM-3为代表的免疫检查点抑制剂虽已改变癌症治疗格局,但仅对15%–40%的患者有效,主要瓶颈在于肿瘤微环境(TME)的免疫抑制状态——尤其表现为T细胞难以进入肿瘤、功能被抑制(即‘冷肿瘤’)。研究团队通过小鼠实验发现,DJ-1不仅是氧化应激感应蛋白,更是一种关键的免疫负调控因子。当DJ-1基因被敲除或被药物(如戒酒药双硫仑)抑制后,肿瘤内的巨噬细胞发生重编程:其活性氧(ROS)水平升高,进而激活NF-κB/STAT3信号通路,促使巨噬细胞向CXCL9阳性(促免疫型)转化,同时减少SPP1阳性(免疫抑制型)巨噬细胞。这类CXCL9+巨噬细胞能分泌趋化因子CXCL9,像‘向导’一样招募并激活CD8+杀伤性T细胞,显著提升T细胞在肿瘤内的数量和功能。尤为关键的是,这种巨噬细胞的转变非常稳定——即使将体外培养的DJ-1缺陷巨噬细胞移植到正常小鼠体内,它们仍能持续激活T细胞。在多种小鼠肿瘤模型(包括对免疫治疗不敏感的‘冷肿瘤’模型)中,联合使用双硫仑与PD-1抗体,比单用PD-1抗体更能抑制肿瘤生长、延长生存期。综上,DJ-1是连接氧化应激与抗肿瘤免疫的关键枢纽;抑制DJ-1不直接作用于T细胞,而是通过‘改造巨噬细胞’这一上游策略,系统性改善肿瘤微环境,为克服免疫治疗耐药提供了安全、可行的新路径。