肠道靶向抗癌诊疗的微型机器人铜基电化学技术
作者: aeks | 发布时间: 2026-03-29 10:00 | 更新时间: 2026-03-29 10:00
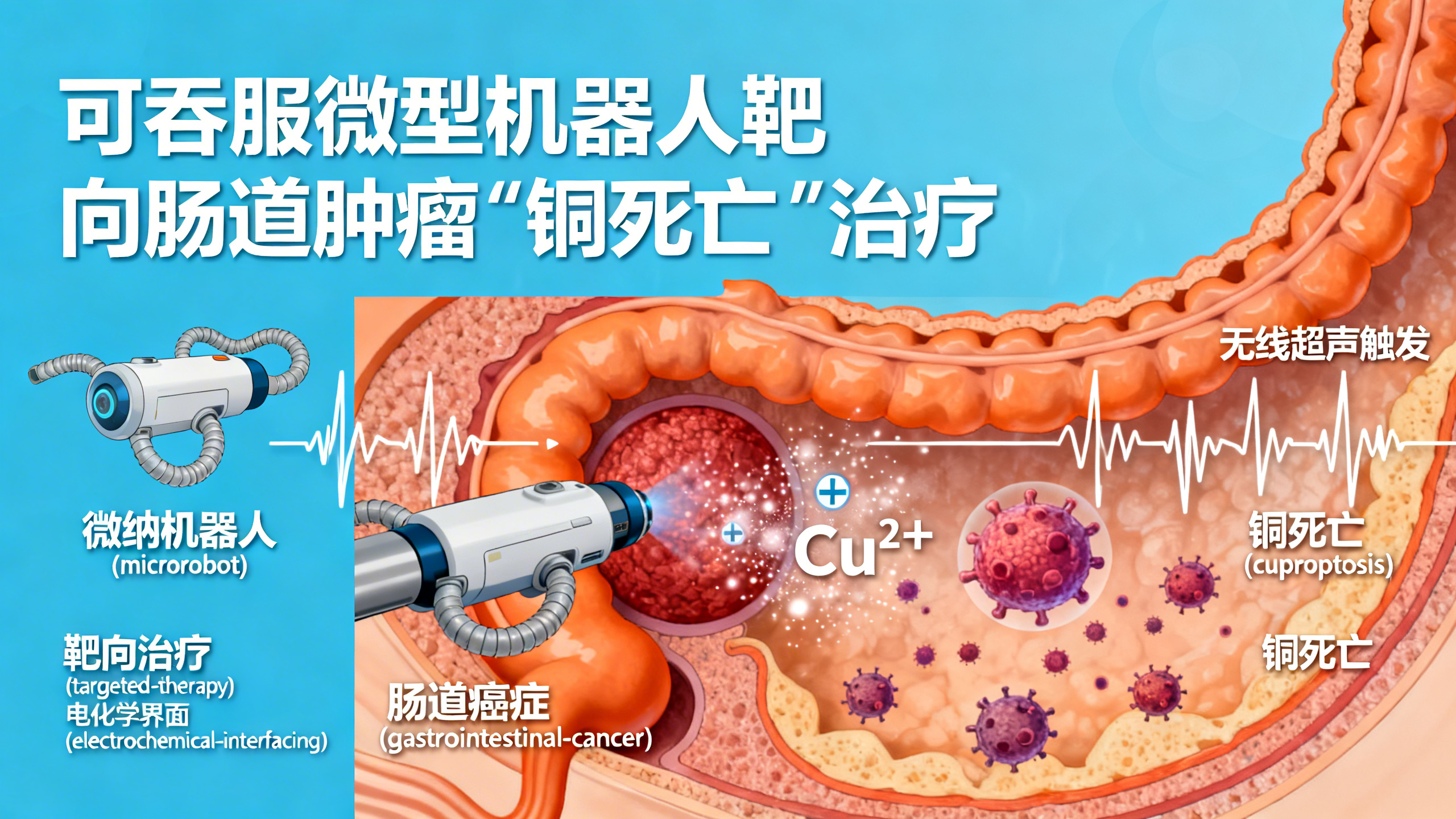
本研究开发了一种面向肠道癌症治疗的创新性口服微纳机器人系统,命名为‘微机器人介导的铜死亡’(M-cuproptosis)。传统抗癌药物在体内分布难以精准控制,尤其在肠道环境中易受血流、黏液屏障和生理清除等干扰,导致药物无法有效富集于肿瘤部位,且深层渗透能力差。本研究突破性地将机械运动、电化学调控与生物化学响应三者协同集成:机器人由磁性软材料制成,可通过外部磁场驱动,在胃肠道内自主滚动、导航并牢固锚定于肿瘤表面;其内置铜储存单元与微型电子电路,在无线聚焦超声(FUS)信号激活下,原位电化学溶解释放铜离子(Cu²⁺);同时,机器人产生的多极电场引导铜离子定向迁移,形成高度浓缩的‘铜离子凝聚云’(Cu-CICs),使肿瘤微环境中的局部Cu²⁺浓度飙升约10⁴倍。这种非扩散主导的主动输运机制,显著提升了铜离子向肿瘤深部的渗透效率——模拟与实验证实,其穿透速度比同等尺寸纳米颗粒快数百至数千倍,可在1小时内使直径达5毫米的肿瘤实现充分饱和。体外实验显示,该技术对包括结直肠癌、胃癌、胰腺癌在内的多种消化道癌细胞均具强效杀伤作用,且机制明确:特异性下调FDX1、LIAS、SDHB等铜死亡关键蛋白,引发线粒体蛋白毒性应激与DLAT寡聚化,确证为经典铜死亡通路。在活体猪肠道模型中,机器人成功完成长距离(约1米)跨器官导航(胃→十二指肠→小肠→结肠)、多点靶向锚定及稳定驻留;在荷瘤小鼠模型中,单次6小时治疗即可近乎完全清除皮下肿瘤,组织学与免疫荧光分析进一步证实了肿瘤结构破坏与铜死亡标志物表达下降。安全性评估表明:机器人采用食品级材料与可降解黏附层,口服后未引起消化道或全身器官炎症或病理改变,血液生化指标均在正常范围;铜载量经精确优化(约0.2毫克),远低于人体每日耐受上限(2%),且释放过程受超声严格按需控制,极大降低了铜过载与脱靶毒性风险。综上,该平台不仅解决了肠道靶向给药的‘定位难、驻留难、渗透难’三大瓶颈,更首次将微型机器人从被动载体升级为主动‘治疗执行器’,为消化道早中期癌症(T1–T3期)提供了一种微创、精准、可编程的全新治疗范式。